আরেক রকম ● দ্বাদশ বর্ষ একবিংশ সংখ্যা ● ১-১৫ নভেম্বর, ২০২৪ ● ১৫-৩০ কার্তিক, ১৪৩১
প্রবন্ধ
মেডিসিনের নোবেলঃ ছোট অণু, বড় আবিষ্কার
স্বপন ভট্টাচার্য
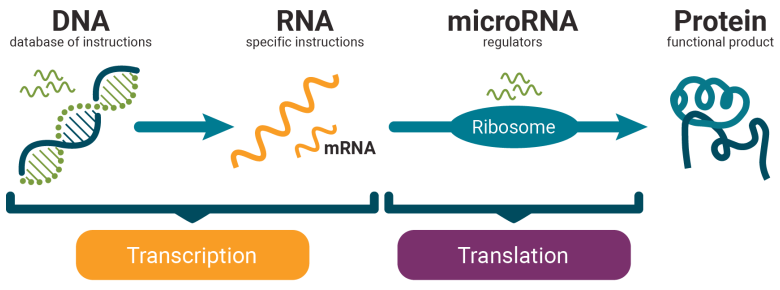
সমস্ত জীবকোষে জীবনের লক্ষ্মণগুলো যে এক অমোঘ সূত্র দ্বারা প্রকাশ করা যেতে পারে তা প্রথম ব্যক্ত করেছিলেন ফ্রান্সিস ক্রিক ১৯৫৭ সালে, তাঁর ‘সেন্ট্রাল ডগমা’ প্রস্তাবনায়। ক্রিক ইতিপুর্বে রবার্ট ডিউয়ি ওয়াটসনের সঙ্গে যৌথভাবে (১৯৫১ সাল সেটা) ডিএনএ (ডি-অক্সিরাইবো নিউক্লিক অ্যাসিড) অণুর বর্ণনা করে দুনিয়াকে জানিয়েছেন জীন জিনিসটার কী কী ভৌত-রাসায়নিক বৈশিষ্ট্য রয়েছে যাতে করে এটা বংশগতির ধারক হয়ে উঠেছে! তার পরেও অবশ্য প্রশ্ন যেটা থাকে তা হল, ডিএনএ বংশগতির খবরটা প্রজন্ম থেকে প্রজন্মান্তরে নিয়ে যায় বটে, কিন্তু সরাসরি কোষীয় স্তরে যে সমস্ত বিক্রিয়া দ্বারা জীবনের প্রকাশ ঘটে তাতে তো অংশ নেয় প্রোটিন, ডিএনএ নয়। ক্রিক সাহেব মোক্ষম অনুমান করেছিলেন যে ডিএনএ-বাহিত ‘বার্তা’ প্রোটিনে রূপান্তরিত হতে পারে যদি এই দুয়ের মাঝে কোনও বার্তাবাহক থাকে। দেখা গেল যথার্থই এক ‘বার্তাবহ’ বা মেসেঞ্জার অণু আছে প্রতিটি কোষে, যারা ডিএনএ-র ভাষাকে প্রোটিনের ভাষায় ‘অনুবাদ’ করতে মধ্যস্থতাকারীর ভূমিকা নেয়। এরা হল আরএনএ (রাইবো নিউক্লিক অ্যাসিড), আরও নির্দিষ্টভাবে বলতে গেলে বার্তাবহ বা মেসেঞ্জার আরএনএ (mRNA)।
জাতে এরা ডিএনএ-এর মতই নিউক্লিক অ্যাসিড বটে, কিন্তু গঠনে একতন্ত্রী, ডিএনএ-এর মতো দ্বিতন্ত্রী অণু এরা নয়। সুতরাং জীবনের কেন্দ্রীয় প্রত্যয় বা সেন্ট্রাল ডগমা হিসাবে এই সত্য অনুধাবন করতে আর কোনও অসুবিধে রইল না যে জীন জিনিসটা ডিএনএ হলেও, সেটির ‘ভাষা’ প্রোটিনের ‘ভাষা’ থেকে একান্তই পৃথক এবং এমনও নয় যে কোষ ডিএনএ-এর ভাষাটিকে নিজের কেরামতিতে প্রোটিনের ভাষায় ‘অনুবাদ’ করে নিতে সক্ষম! কোষ সেটা পারে যদি ডিএনএ দ্বারা পরিবাহিত ‘বার্তা’-র একটা ট্রান্সক্রিপশন বা লিপান্তর ঘটে ওই বার্তাবহ mRNA-এর ‘লিপি’-তে, কারণ কোষে প্রোটিন তৈরির কাজটা হয় mRNA-এর ‘লিপি’-কে অথবা ট্রান্সস্ক্রিপ্ট-কে প্রোটিনের ‘লিপি’তে অনুবাদ করে। ডিএনএ থেকে ট্রান্সক্রিপশন পদ্ধতিতে বার্তাবহ বা mRNA তৈরি করা এবং তার পরবর্তী ধাপে mRNA-এর বার্তা-কে প্রোটিনে অনুবাদ বা ট্রান্সশ্লেসন করে ফেলা নির্ভুলভাবে - এই হল জন্মের শুভক্ষণটি থেকে শুরু করে চিরনিদ্রায় ঢলে পড়ার আগে পর্যন্ত এককভাবে একটি সক্রিয় কোষের অথবা অনেক সক্রিয় কোষের আধার একটি জীবের তথাকথিত বেঁচে থাকার চাবিকাঠি।
পরবর্তীকালে এটাও প্রতীয়মান হয় যে শুধু বার্তাবহ বা mRNA নয়, প্রোটিন তৈরির এই কারিগরিতে আরও বেশ কয়েকরকম আরএনএ যেমন, রাইবোজোমাল RNA (rRNA) বা ট্রান্সফার RNA (tRNA) ইত্যাদি সমগুরুত্বের অণুরও ভূমিকা আছে। এছাড়াও, ইতোমধ্যেই জানা গিয়েছিল যে কিছু কিছু ভাইরাস সম্পূর্ণভাবে ডিএনএ-বিহীন এবং তাদের ক্ষেত্রে জীন বলতে ওই আরএনএ-কেই বুঝি আমরা। বস্তুত, আদি পৃথিবীতে প্রাণের বিবর্তনে আরএনএ এসেছিল আগে এবং তার অনুসারী হয়ে ডিএনএ - এমনটা বিশ্বাস করার মতো প্রামাণ্য যুক্তিও রয়েছে।
যাই হোক, জীনের চরিত্র বা কাজ করার রহস্য পুরোপুরি উন্মোচিত হলেও যে প্রশ্ন থেকেই যায় তা হল, এই জীন বস্তুটিকে নিয়ন্ত্রণ করে কে? প্রতিটি কোষ এককভাবে ঠিক সময়ে ঠিক কাজটা করে বলেই না এককোষী জীব থেকে শুরু করে কোষসমষ্টির সমন্বয়ে গঠিত একটা জীবদেহ সম্পূর্ণরূপে বিকশিত হতে পারে। মানুষের শরীর থেকেই একটা উদাহরণ দিয়ে দেখা যেতে পারে কোষের ঠিক সময়ে ঠিক কাজ বলতে ঠিক কী বোঝায় এবং তার গুরুত্ব কতটা!আমরা জানি, পুরুষ বা নারীশরীরে বয়ঃসন্ধিকালে যে পরিবর্তনগুলি আসে তা প্রাথমিক ও গৌণ যৌনতা নির্ণায়ক। কিছু সুনির্দিষ্ট জীন এই বিশেষ বয়ঃক্রমে সক্রিয় হয়ে ওঠে বলেই এই পরিবর্তন মানবদেহের বৃদ্ধি এবং বিকাশের (growth and development) এত গুরুত্বপূর্ণ একটি পর্যায় বলে বিবেচিত হয়। কিন্তু বয়ঃপ্রাপ্তির এই বার্তা যে কোনও সুস্থ ও স্বাভাবিক মানুষের শরীরে তো জন্ম থেকেই আছে। এমন তো নয় যে, সেই বিশেষ বয়সে তার দেহে বাইরে থেকে কিছু জীন এসে পৌঁছালো! যে সব জীনের সক্রিয়তায় বয়ঃসন্ধিকালে এই বহিঃপ্রকাশ, তারা জন্ম থেকেই ডিএনএ-বাহিত বার্তা নিয়ে বাবা-মা’র থেকে অপত্যে এসে পৌঁছেছে, কিন্তু তাদের প্রকাশিত হবার টাইমিং একেবারে প্রোগ্রামড্ বলা যায়। এই প্রোগ্রামিংটা না থাকলে কন্যাসন্তান জন্মের পরেই ঋতুমতী হয়ে পড়তে বাধা ছিল না কারণ অপরিণত ডিম্বাণু নিয়েই সে জন্মায়, কিন্তু পরিণতিপ্রাপ্তির জন্য প্রয়োজনীয় জীনগুলির সক্রিয়তা সুনির্দিষ্ট সময়চক্রে বাঁধা বলেই সেটা হয় না। একইভাবে ফুল ফোটে, পিউপা প্রজাপতি হয়, পাখি ডিম পাড়ে বৃদ্ধিচক্রের একটি সুনির্দিষ্ট সময়ে, যদিও খবরগুলো প্রাণসঞ্চারের মুহূর্ত থেকেই থাকে ওই ডিএনএ-তে। আমাদের রোগ বালাইয়ের অনেকটাও এই জীন দ্বারা নিয়ন্ত্রিত কাজগুলোর ওপর নিয়ন্ত্রণের অভাবসঞ্জাত। আবার একটা উদাহরণ দেখতে পারি; আমাদের কেটে-ছড়ে গেলে চামড়ার কোষগুলো বিভাজিত হয়ে ক্ষতটা বুজিয়ে দিলেই আমরা বলি নিরাময় ঘটেছে। নিরাময়ের জন্যই বিভাজনে প্রোগ্রামড্ এই পরিণত কোষেরা। কিন্তু মনে করুন, নিয়ন্ত্রণের অভাবে কোষগুলো নিরাময়ের পরেও আপন খেয়ালে বিভাজিত হয়ে চলল। এমনটা হলে যেটা ঘটবে তা হল দেহের বাকি অংশের সঙ্গে সামঞ্জস্যবিহীন একটা ক্রমবর্ধমান কোষসমষ্টি, যাকে 'টিউমার' বলা যেতে পারে এবং যা ক্যান্সারের সূচনা বলে পরে শনাক্ত হতেও পারে।
এই যে নিরাময়ের কাজ শেষে বিভাজন থেমে যাওয়া, এটা কোষচক্রের ওপর একটা নিয়ন্ত্রণ থাকে বলেই সম্ভব হয়। একই কারণে, বয়ঃপ্রাপ্তি, ফুল ফোটা, পিউপা থেকে প্রজাপতির উড়ান বা পাখির ডিম পাড়া সবই ঠিক সময়ে ঠিক জীনের সুইচ অন বা সুইচ অফ হয়ে যাবার কারণে ঘটে থাকে। এবং প্রকৃতির এই বিপুল জীববৈচিত্র আদতে জীবকোষে বংশানুক্রমে পরিবাহিত ‘বার্তা’ এবং সেই বার্তা প্রকাশের সুনিয়ন্ত্রিত নিয়ম - এই দু'য়ের সমন্বয়।
জীন নিয়ন্ত্রণের অনেক পদ্ধতি রয়েছে যা বিস্তারিতভাবে এই আলোচনার বিষয় নয়, কিন্তু অনুমান করতে পারা কঠিন নয় যে জীন যেহেতু বার্তাবহ আরএনএ-এর মাধ্যম-ব্যতীত ‘প্রকাশিত’ হতে পারে না, সেহেতু ‘জীন নিয়ন্ত্রণ’ (Gene Regulation)-এর একটা বড়ো চাবিকাঠি হল mRNA বা ট্রানস্ক্রিপ্ট তৈরি হওয়া নিয়ন্ত্রণ। আবার ট্রানস্ক্রিপ্ট তৈরি হবার পরেও সেটি অনূদিত হয়ে প্রোটিন তৈরি করার পথেও এই নিয়ন্ত্রণ আসতে পারে। একে বলে পোস্ট-ট্রানস্ক্রিপশনাল রেগুলেশন।
২০২৪-এর মেডিসিন তথা শারীরবিজ্ঞানে নোবেল পুরষ্কার এসেছে নতুন এক ধরনের আরএনএ আবিষ্কার এবং পোস্ট-ট্রানস্ক্রিপশনাল রেগুলেশনে তাদের ভূমিকা নির্ণয়ে মৌলিক অবদান রাখার জন্য ম্যাসাচুসেটসের ভিক্টর অ্যামব্রোজ এবং গ্যারি রাভকুন-এর হাতে। ১৯৯৩ সালে, তাঁরা উভয়ে আলাদা আলাদাভাবে কাজ করতে গিয়ে অতি ক্ষুদ্র এক ধরনের আরএনএ অণুর হদিশ পেয়েছিলেন যাদের বলে মাইক্রো আরএনএ (miRNA) এবং পরবর্তীকালে পরিষ্কার হয় যে, এই miRNA, জীনের প্রকাশ নিয়ন্ত্রণে গুরুত্বপুর্ণ ভূমিকা নেয় গবেষণাগারে এবং প্রকৃতিতেও।
মাইক্রো RNA আবিষ্কার
উন্নততর এবং জটিল দেহগঠনবিশিষ্ট জীবদেহের জীনচরিত্র বোঝা এবং কার্যকারিতা অনুধাবনের জন্য C. elegans (Caenorhabditis elegans) নামের একটা সুতাকৃমির গবেষণাগারে ব্যবহারের ইতিহাস পঞ্চাশ বছরেরও বেশি পুরোনো। মিউটেশনের মাধ্যমে এদের জীনতন্ত্রে পরিবর্তন আনাটা অপেক্ষাকৃত সহজ এবং নানা রকমের মিউটেশন-সঞ্জাত গঠনগত ও শারীরবৃত্তীয় পরিবর্তন সাদা চোখেই ধরা পড়ে। এই কৃমির lin-4 নামাঙ্কিত একটা জীনের মিউটেশনে কৃমিটার লার্ভা দশা থেকে পরিণতি প্রাপ্তির পথে অনেক অসম্পূর্ণতা চোখে পড়ে। অনেক ধরনের কোষ যা স্বাভাবিকভাবে থাকা উচিৎ তা এদের নেই; স্ত্রী যৌনাঙ্গ গঠনগত পরিণতি পায় না অথচ ডিম তৈরি হয়ে চলে, ফলে দেহাভ্যন্তরে ডিম জমে যেতে থাকে। এর কিছুদিন পরে ঐ একই গবেষণাগারে lin-14 নামাঙ্কিত অপর একটা জীনের আর একটা মিউট্যান্ট খুঁজে পাওয়া যায়। এটিরও পরিণতিপ্রাপ্তির পথে অনেক সময়-বিপর্যয় ঘটে, কিন্তু বিপর্যয়ের প্রকৃতিটা lin-4-এর বিপরীতধর্মী। এদের বলে হেটেরোক্রনিক মিউট্যান্ট অর্থাৎ পরিণতিপ্রাপ্তির পথে যাদের জীন প্রকাশের টাইমিং এলোমেলো হয়ে গেছে।

ভিক্টর অ্যামব্রোজ পিএইচডি করেছিলেন বিখ্যাত নোবেল লরিয়েট ডেভিড বাল্টিমোরের (১৯৭৫) কাছে পোলিও ভাইরাসের জেনেটিকস নিয়ে, আর পোস্ট-ডক ফেলো হিসেবে যোগ দিলেন আর এক নোবেল লরিয়েট রবার্ট হরভিৎসের (২০০২)-এর ল্যাবে। ভাইরাস জিনোম ছেড়ে উচ্চতর প্রাণীর জিনোম গবেষণায় এসে আবিষ্কার করলেন যে lin-4 এবং lin-14-এর পারস্পরিক বৈপরীত্য বস্তুত একসূত্রে গাঁথা। কী ভাবে তা সম্ভব? ভিক্টর অ্যামব্রোজ দেখেছিলেন যে এদের মধ্যে প্রথমটি, দ্বিতীয়টির প্রকাশকে নিয়ন্ত্রণ করে। নিয়ন্ত্রণ মানেই যে আবশ্যিকভাবে জীনের প্রকাশ তা কিন্তু নয়, বরং বহু জীন নিয়ন্ত্রিত হয় প্রকাশকে দমিয়ে রেখে। এই ধরনের নিয়ন্ত্রককে বলে নেগেটিভ রেগুলেটর। ভিক্টর অ্যামব্রোজ বললেন lin-4 হল lin-14 জীনের নেগেটিভ রেগুলেটর। lin-14 মিউট্যান্টকে লার্ভা দশায় বেঁধে রেখে পরিণতিতে না পৌঁছাতে দেবার কাজ করে lin-4।

গ্যারি রাভকুন ডক্টরাল কাজ করেছিলেন 'হাভার্ড মেডিক্যাল স্কুল'-এ ফ্রেডেরিক অসুবেল-এর ল্যাবে। পোস্ট-ডক ফেলো হিসাবে তিনিও আশির দশকের গোড়ায় যোগ দিলেন রবার্ট হরভিৎসের টিমে। এরপর দু’জনেরই দীর্ঘ যাত্রা শুরু হয় সুতো কৃমি জেনেটিকসে যদিও সহযাত্রা তা নয় অন্তত প্রথমাবস্থায়। অ্যামব্রোজ ম্যাসাচুসেটসে এবং রাভকুন হার্ভার্ডে শিক্ষকতায় এলেন এবং গড়ে তুললেন নিজের নিজের গবেষণাগার। অ্যামব্রোজ lin-4 জীন-এর ট্রানস্ক্রিপ্টটি পরীক্ষা করতে গিয়ে দেখলেন এটি থেকে আদপেই কোন প্রোটিন তৈরি হয় না - অর্থাৎ এই ট্রানস্ক্রিপ্ট RNA বটে, কিন্তু প্রোটিন তৈরির নিমিত্ত কোনও বার্তা এটি বহন করছে না। RNA গঠিত হয় মালার মতো সাজানো বহুসংখ্যক ‘বেস’ দিয়ে। বেসগুলোর ধরণ কেবল দুই জোড়া, কিন্তু সংখ্যায় কত তা নির্ভর করে কোন জীব, কোন জীন, তার উপর। যেমন ধরুন মানুষের এক একটি কোষে প্রাপ্ত ডিএনএ-তে মোট বেসের সংখ্যা তিনশো কোটির বেশি। একক জীনের কথাই যদি ধরা যায়, মানুষের এক TTN ট্রান্সক্রিপ্টটাই (যা টাইটিন নামের একটা প্রোটিন তৈরির জন্য বার্তাবহ) হল ১,১৮,৯৭৬ বেস লম্বা। তুলনায় lin-14 তো অতি ক্ষুদ্র, বিশ বাইশটা মাত্র বেস দিয়ে তৈরি এটা এবং প্রোটিনের জন্য কোনও বার্তা সেটি বহন করছে না। যথার্থই মাইক্রো এটা গঠনে, এবং মাইক্রো RNA (miRNA) নামকরণে কোন দ্বৈততার অবকাশই নেই।
অপরদিকে lin-14 ট্রানস্ক্রিপ্ট বেস-বিন্যাসটি পড়ে ফেলতে সক্ষম হলেন রাভকুন। পড়ে ফেলার এই পদ্ধতিটি, যার পোষাকি নাম 'সিকোয়েন্সিং'; এর সঙ্গে আজকাল কমবেশি অনেকেই পরিচিত। যাই হোক, অ্যামব্রোজ ও রাভকুন নিজেদের মধ্যে সিকোয়েন্স ডেটা এক্সচেঞ্জ করলেন ১৯৯২ সালে, এবং অবাক হয়ে দেখলেন lin-14 ট্রানক্রিপ্টের একটা ছোট্ট অংশের সঙ্গে lin-4 ট্রান্সক্রিপ্টের একটা পরিপূরকতা আছে। পরিপূরকতা বা কমপ্লিমেন্টারিটি হল, যে দু’জোড়া বেস দিয়ে জীবনের ভাইটাল অনুদ্বয় গঠিত সেই বেসগুলোর মধ্যে জোড় বাঁধার শর্ত। বস্তুত, কৃমিতে জরুরী প্রোটিন তৈরির জন্য একান্ত দরকারি ট্রানস্ক্রিপ্ট lin-14-এর কাজ শুরুর বেসগুলোর সঙ্গে জোড় বেঁধে বসে থাকে lin-4 মাইক্রো আরএনএ। ফলে সেটা অকার্যকরী থেকে যায়। এর ফল? lin-14 মিউটান্টগুলো লার্ভা স্তরই পেরোতে পারে না। অপরিণত থেকে যায়। সুতরাং, এই বিজ্ঞানীদ্বয়ের চেষ্টায় যেটা হল, তা কেবল এই আবিষ্কার নয় যে জীবকোষে এমন কিছু আরএনএ থাকা সম্ভব যারা অতি ক্ষুদ্র (miRNA) এবং যাদের ক্ষমতা আছে জীনের কাজ করার ক্ষমতাকে নিয়ন্ত্রণ করার। পরবর্তীকালে দেখা যায়, শুধু কৃমি নয়, মানুষে ও উদ্ভিদে miRNA আছে এবং জীন রেগুলেশনে তারা পজিটিভ এবং নেগেটিভ - উভয় ধরনের ভূমিকাই পালন করে। শুধু মানুষেই ৩,০০০-এর বেশি miRNA সম্পর্কে ডেটাবেস তৈরি হয়েছে যাদের ভূমিকা আজকের দিনে চর্চিত গবেষণার বিষয়। জীন সাইলেন্সিং (অর্থাৎ জীনকে অকার্যকরী করে ফেলা) যে মাইক্রো RNA কাজ করার একটা চালু পদ্ধতি তাতে কোনও সন্দেহ নেই, কিন্তু সব সময়ে যে সেটা একের বিরুদ্ধে এক তা না’ও হতে পারে। একটিমাত্র মাইক্রো RNA যেমন অনেকগুলো জীনকে অকেজো করে রাখতে পারে, তেমনই অনেকগুলো মাইক্রো RNA মিলে একটা জীনকে বসিয়ে রাখে, তা’ও দেখা গেছে। সব সময় যে সুইচ অফ করে দেওয়া তা নয়, কোনও কোনও সময় মাইক্রো RNA বার্তাবহ ট্রানস্ক্রিপ্টকে খণ্ডিত করে ফেলতেও পারে।
মাইক্রো RNA ও ক্যান্সার
ক্যান্সারে মাইক্রো RNA-এর গুরুত্ব জানা যায় প্রথমবার ২০০২ সালে যখন ক্রনিক লিম্ফ্যাটিক লিউকেমিয়া (CLL) রোগীদের ক্ষেত্রে দুটি মাইক্রো RNA মানবশরীরের ১৩ এবং ১৪ নম্বর ক্রোমোজোম থেকে অপসারিত দেখা যায়। এটা নিঃসন্দেহে একটা পজিটিভ রেগুলেশনের উদাহরণ, কারণ ওই বিশেষ দু’টি (এদের নাম দেওয়া হয়েছে miR15 এবং miR16) যতক্ষণ স্বাভাবিক দেহে স্বাভাবিক অবস্থানে আছে ততক্ষণ ওরা টিউমার সাপ্রেসর বা টিউমার অবদমক।
এছাড়া মাইক্রো RNA অঙ্কোজীন নিয়ন্ত্রক হিসেবেও কাজ করতে পারে। অঙ্কোজীন হল ক্যান্সার সৃষ্টিকারী জীন। ফুসফুসের ক্যান্সারে আক্রান্ত মানুষের ক্ষেত্রে দেখা যাচ্ছে let-7 নামাঙ্কিত একটা মাইক্রো RNA স্বাভাবিকের তুলনায় কম পরিমাণে পাওয়া যায়। এই মাইক্রোটির মানুষের কোষে RAS নামক একটি অঙ্কোজীনকে বেঁধে ফেলার প্রবণতা আছে। সুতরাং, এটা নেগেটিভ রেগুলেটরের কাজ করে, কিন্তু মানুষের পক্ষে তার ফলাফল তো অবশ্যই পজিটিভ, কেন না যার let-7 মাইক্রো RNA পরিমাণ স্বাভাবিক, তার ফুসফুস ক্যান্সারের জন্য দায়ী RAS জীনটি প্রকাশিত হতে পারে না। উল্টোটাও হয়। ইঁদুরে গবেষণায় দেখা গেছে, miR21 নামের মাইক্রো RNA বেশি পরিমাণে উৎপাদিত হলে (ওভার-এক্সপ্রেশন) টিউমার হচ্ছে, আবার এটা তৈরি করার জীনটাকেই যদি ছেঁটে বাদ দেওয়া যায় তাহলে টিউমারের বৃদ্ধি কমে যাচ্ছে। অর্থাৎ, ক্যান্সার সৃষ্টি বা অবদমন দুই’ই নিয়ন্ত্রণে মাইক্রোদের বেশ উল্লেখযোগ্য ভূমিকা আছে। ক্যান্সার-এর সব থেকে খারাপ অবস্থাটা হল 'মেটাস্ট্যাসিস' দশায় পৌঁছানো, যার ফলে দেহের এক জায়গা থেকে স্থানান্তরিত টিউমার কোষ, নতুন জায়গায় টিউমার তৈরির কাজ শুরু করে দেয়। মাইক্রোদের এক্ষেত্রে ভূমিকার দু’টো দিকের কথাই জানা গেছে। MiR-10b হল তেমন একটি মাইক্রো RNA যা মেটাস্ট্যাসিস অ্যাকটিভেটর হিসেবে কাজ করে অর্থাৎ টিউমার কোষকে নতুন জায়গায় প্রতিস্থাপিত হতে সহায়তা করে। অন্য দিকে, স্তন ক্যান্সার মেটাস্ট্যাটিক হয়ে ওঠার পথে বাধা হয়ে দাঁড়ায় miR-335, miR-126 ইত্যাদির মতো মাইক্রোরা।
হৃদযন্ত্রের সমস্যায় মাইক্রো RNA
কার্ডিওমায়োসাইট্স হল হৃদযন্ত্রের পেশীর কোষ যাদের কাজ করা বা ভুল কাজ করায় মাইক্রোদের ভূমিকার সুস্পষ্ট প্রমাণ পাওয়া গেছে। MiR-1 হল এমন একটা মাইক্রো RNA যা ইঁদুরে কার্ডিওমায়োসাইট্স-এর কার্যকারিতা হ্রাস করায়। অপরপক্ষে miR-195-এর ওভার-এক্সপ্রেশনের জন্য ইঁদুর মডেলে হার্ট ফেইল হতে দেখা গেছে। গত কয়েক বছরের গবেষণায় এটাও দেখা গেছে যে হৃদযন্ত্র অস্বাভাবিক বড় হয়ে যাওয়ার ঘটনায় miRNA-গুলির ভূমিকা আছে। এক্ষেত্রে এরা পজিটিভ রেগুলেটর, তাই হৃদযন্ত্রের কোষের সংখ্যা অস্বাভাবিকভাবে বাড়তে থাকে, তবে তার ফল হৃদয়ের অধিকারিটির ওপর আদৌ সুখকর হয় না।
অটো-ইমিউন রোগে মাইক্রো RNA
ছুলি থেকে শুরু করে চামড়ার ক্যান্সার - নানা রকম রোগ সৃষ্টি হতে পারে miRNA দ্বারা জীন নিয়ন্ত্রণের ফলে। miR-203 হল এমন একটা মাইক্রো যা কেরাটিনোসাইটস নামক চামড়ার কোষকে অধিক মাত্রায় সক্রিয় করে তোলে, যার জন্য ছুলি হয়। রিউমাটয়েড আর্থ্রাইটিস বা SLE (সিস্টেমিক লুপাস ইরাইথেম্যাটোসাস) হল এমন রোগ যেখানে শরীরের ইমিউন সিস্টেম নিজের দেহকোষগুলোকেই ব্যাকটেরিয়া ভাইরাসের মতো প্রতিপক্ষ ভেবে আক্রমণ করে বসে। SLE রোগের ক্ষেত্রে miR-21 এবং miR-148a - এই দুটো মাইক্রো RNA আক্রমণকারী কোষগুলোর মধ্যে ওভার-এক্সপ্রেসড হয়। দেখা গেছে দু’টি রেসিয়াল গ্রুপ, যথাক্রমে আফ্রিকান আমেরিকান এবং ইউরোপিয়ান আমেরিকানদের মধ্যে অটো-ইমিউন নেফ্রাইটিসের ক্ষেত্রে একগুচ্ছ মাইক্রো RNA সম্পূর্ণ পরস্পর বিপরীতধর্মী ব্যবহার দেখায়। প্রথমটায় নেগেটিভ হলে দ্বিতীয়টায় তা পজিটিভ রেগুলেটর।
নিউরো-ডিজেনারেটিভ রোগে মাইক্রো RNA
অ্যালঝাইমার বা পার্কিনসনস বা হান্টিংটন ডিজিজের মতো রোগ, যেগুলি স্নায়ুতন্ত্রের ক্ষয়জনিত রোগ, তারা বেশ কয়েক রকম miRNA বেশি বা কম সক্রিয়তার সঙ্গে সরাসরি যুক্ত। বয়সের সঙ্গে সঙ্গে যাদের দেহে miR-9, miR-25b এবং miR-128-এর উচ্চতর মাত্রায় প্রকাশ বা ওভার-এক্সপ্রেশন এবং miR-124a-এর হ্রাস বা ডাউন-রেগুলেশন অ্যালঝাইমার ডিজিজের জন্য যে দায়ী তা গবেষণাগারে প্রমাণিত হয়েছে। এই মাইক্রোগুলির উপস্থিতি রক্তে বা কোষকলায় মার্কার হিসাবে সনাক্ত করার কাজটা খুব সহজ নয়। ক্যান্সার কোষ যেমন সহজেই পাওয়া যায় দেহ থেকে, মস্তিস্ক থেকে বা নার্ভ থেকে ততটা নয়। কীভাবে তা সহজতরভাবে করা যায়, তা আপাতত একটা চ্যালেঞ্জ বটে, তবে সময়ের সঙ্গে সঙ্গে অনেক অগ্রগতির অবকাশ আছে এই গবেষণায়!
ব্যবহারিক সম্ভাবনা
যদি সত্যি সত্যিই কোনও কোনও প্রাণঘাতী রোগ মাইক্রো আরএনএ-এর ওভার-এক্সপ্রেশনের জন্য হতে পারে, তা হলে তাদের জন্যও বিপরীতধর্মী ক্ষুদ্র অ্যান্টি-আরএনএ ব্যবহার করা যায় কি না তা নিয়ে কিছু কাজ হয়েছে, কিছু অগ্রগতিও হয়েছে। এদের বলা হয় অ্যান্টিগোমির (Antigomir) এবং কোলেস্টেরল দিয়ে প্যাক করে এই অতি ছোট অ্যান্টি-miRNA দিয়ে ক্যান্সার নিয়ন্ত্রণের চেষ্টা হচ্ছে। এছাড়া মাইক্রো RNA সংশ্লেষের বিভিন্ন ধাপ ব্লক করে সেটির উৎপাদনটাই ক্ষেত্রবিশেষে কমিয়ে দেওয়া যায় কি না তাও বোঝার চেষ্টা হচ্ছে। আংশিক সফল এই গবেষণা ক্যান্সার থেরাপিতে নতুন এক মোড়। ঠিক বিপরীতভাবে, যেখানে কম মাইক্রো RNA তৈরিটাই বিপত্তির কারণ সেখানে বাইরে থেকে প্রয়োগ করে সাফল্য পাওয়ার কিছু নজির রয়েছে। এগুলো এখনও পর্যন্ত গবেষণাগারের সাফল্যের খতিয়ান। মাইক্রো RNA আবিষ্কার এবং সেটি দ্বারা পোস্ট-ট্রান্সক্রিপশনাল রেগুলেশন - হাত ধরাধরি করে চলা এই যৌথ আবিষ্কারের জন্যই এবারের নোবেল সম্মান পেলেন ভিক্টর অ্যামব্রোজ ও গ্যারি রাভকুন।
তথ্যসূত্রঃ
1. Rickard Sandberg. (2024). For the discovery of microRNA and its role in post-transcriptional gene regulation. https://www.nobelprize.org/uploads/2024/10/advanced-medicineprize2024-2.pdf
2. Leigh-Ann MacFarlane, Paul R Murphy (2010). MicroRNA: Biogenesis, Function and Role in Cancer. Current Genomics 2010 Nov; 11(7):537-561. doi: 10.2174/138920210793175895.
3. Almeida, Maria I et al (2011). MicroRNA history: Discovery, recent applications and next rontiers. https://api.core.ac.uk/oai/oai:repositorium.sdum.uminho.pt:1822/18666
চিত্রঋণঃ অন্তর্জাল থেকে প্রাপ্ত।

